- A+
N-溴代琥珀酰亚胺(NBS)
N-溴代琥珀酰亚胺(NBS)是一种溴化和氧化剂,在自由基反应(例如:烯丙基溴化物)和各种亲电子添加剂中用作溴的来源。NBS溴化底物如醇和胺,然后在碱存在下消除HBr,产生净氧化产物,其中未掺入溴。
名称反应
Wohl-Ziegler反应
近期文献

已经开发了一种有效且用户友好的方法,用于使用β-环糊精(β-CD)在水中用N-溴代琥珀酰亚胺(NBS)氧化脱保护四氢吡喃基(THP)醚 。一系列四氢吡喃醚在室温下以令人印象深刻的产率进行氧化脱保护。
M. Narender,MS雷迪,KR饶,合成,2004年,1741年至1743年。

N-烷氧基酰胺通过氧化均偶联和随后的热脱氮,在NBS在甲苯中的存在下方便地得到相应的羧酸酯。甚至具有大体积或长链取代基的底物也在这种方便和经济的方法中以良好的收率得到产物,以直接将烷氧基酰胺部分转化为羧酸酯官能团。
N. Zhang,R。Yang,D。Zhang-Negrerie,Y。Du,K。Zhao,J。Org。化学。,2013, 78,8705-8711。

用N-溴代琥珀酰亚胺和I 2 -水NH 3
S 将乙基芳烃直接转化为伯芳香酰胺.Shimokawa,Y。Kawagoe,K。Moriyama,H.Togo ,Org。快报。,2016,18,784-787。

硼酸与氰酰胺基/芳基氰基酰胺基的有效,金属和无碱的化学选择性反应在环境温度下在1小时内提供伯芳基,杂芳基和烷基胺。该反应由PIFA和NBS介导。
N. Chatterjee,M。Arfeen,PV Bharatam,A。Goswami,J.Org。化学。, 2016, 81,5120-5127。
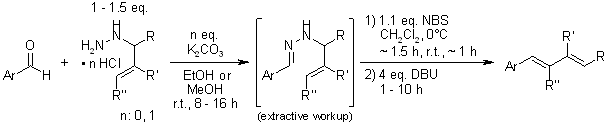
由醛和N-烯丙基肼衍生物立体选择性合成二烯,为各种底物提供高水平的(E)- 立体选择性。向反应混合物中加入亲二烯体允许单瓶二烯合成 - 环加成序列。
DA Mundal,KE Lutz,RJ Thomson,Org。快报。,2009年, 11,465-468。

在N-溴代琥珀酰亚胺存在下 用MoO 2 Cl 2实现β-羟基羰基化合物向α-溴化1,3-二羰基化合物的有效一锅转化。所有反应均在温和条件下进行,并提供良好的收率。在苄基和烯丙基位置不发生溴化。 K·杰亚库马尔,DK昌德,合成,2009年,306-310。

K·杰亚库马尔,DK昌德,合成,2009年,306-310。

在非常温和的条件下,在廉价的卤化试剂如N-溴代琥珀酰亚胺和N-氯代琥珀酰亚胺和FI-750-M作为两亲物的存在下,在水中实现了炔烃的选择性氧卤化反应。没有检测到芳环上的卤化。反应介质和催化剂可以循环使用。
L. Finck,J。Brals,B。Pavuluri,F。Gallou,S。Handa,J。Org。化学。,2018,83,7366-7372。

在二异丁基氢化铝和(Ni(dppp)Cl 2)存在下进行可靠的,操作简单的催化α-选择性氢化铝化反应,并且与未催化的转化不同,产生很少或不产生炔基铝副产物。衍生的α-乙烯基卤化物和硼酸酯可以通过用适当的亲电子试剂直接处理来合成。
F. Gao,AH Hoveyda,J。Am。化学。SOC。,2010, 132,10961-10963。

通过在卡宾中心串联的两个独立离子物质以分子间方式捕获重氮物质将亲电子试剂和亲核试剂安装在相同的碳上。这种无金属概念能够区域选择性合成各种乙烯基卤化物,乙烯基砜和炔烃衍生物。
DP Ojha,KR Prabhu,Org。快报。, 2015年, 17,18-21。

不饱和化合物如烯烃,炔烃,丙二烯和亚甲基环丙烷(MCP)可在室温下在几分钟内被NBS和溴化锂在THF中二溴化,在温和条件下以良好至极好的产率。
L.-X. 邵M.施,SYNLETT, 2006年,1269年至1271年。

L.-X. 邵M.施,SYNLETT, 2006年,1269年至1271年。

L.-X. 邵M.施,SYNLETT, 2006年,1269年至1271年。

N-溴代琥珀酰亚胺 的使用使得能够从容易获得的苄基仲醇和胺合成药学上重要的α-氨基酮的无金属一锅法策略。该反应通过三个连续步骤进行,包括醇的氧化,酮的α-溴化和α-溴酮的亲核取代,得到α-氨基酮。
S. Guha,V。Rajeshkumar,SS Kotha,G。Sekar,Org。快报。, 2015年, 17,406-409。

N-溴代酰亚胺和DBU的 组合使得烯烃的烯丙基胺化反应成为可能,其中内部和外部氮亲核试剂可以直接安装。DBU对NBS或NBP的双重活化导致更多的亲电子溴和更多的亲核氮原子同时存在。该方案在温和条件下提供了对烯丙基胺化的补充途径。
Y. Wei,F。Liang,X。Zhang,Org。快报。,2013, 15,5186-5189。

报道了一种方便有效的亚烷基环丙烷氨基溴化方法。这通过使用对甲苯磺酰胺和N-溴代琥珀酰亚胺(NBS)分别作为氮和溴源的立体选择性制备N - [(Z)-3-溴丁-3-烯-1-基] - 对甲苯磺酰胺来举例说明。。 X. Huang,W.-J。福, 合成,2006年,1016-1017。

在仅使用少量过量的N-溴代琥珀酰亚胺溴化苄基化合物的连续流动方案中,使用基于透明氟化乙烯聚合物的简单流动反应器设计,用易于获得的家用紧凑型荧光灯(CFL)激活自由基反应。管道。所有反应均使用乙腈作为溶剂进行,因此避免了有害的氯化溶剂如CCl 4。
D. Cantillo,O。de Frutos,JA Rincon,C。Mateos,CO Kappe,J.Org。化学。,2014, 79,223-229。

使用N-溴代琥珀酰亚胺在四丁基溴化铵中实现了高度区域选择性溴化活化的芳族化合物。活性芳烃的主要 对位选择性单溴化,在加入酸性蒙脱土K-10粘土时,在有或没有微波辅助的情况下对反应性较低的底物的速率加速是该方案的显着特征。
NC Ganguly,P。De。S.杜塔,合成,2005年,1103年至1108年。

使用六氟异丙醇作为溶剂能够以良好的收率温和和区域选择性地卤化各种芳烃和杂环与N-卤代琥珀酰亚胺。此外,该方法的多功能性通过开发一锅顺序二卤化和卤化 - Suzuki交叉偶联反应来证明。
R.-J. Tang,T。Milcent,B。Crousse,J。Org。化学。, 2018,83,930-938。

在二咪唑鎓盐存在下,带有给电子配位基团的芳烃的 高度对位选择性卤化,以良好的收率得到对 -芳烃。提出了一种合理的催化反应机理。
J.陈X.雄,陈Z.,J.黄, SYNLETT,2015年,26,2831年至2834年。

通过在浓硫酸中用N-溴代琥珀酰亚胺(NBS)处理,高度失活的芳族化合物顺利地单溴化。温和的反应条件和简单的后处理为以合理的收率合成失活的芳族化合物的溴化合物提供了实用且商业上可行的途径。
K. Rajesh,M。Somasundaram,R。Saiganesh,KK Balasubramanian,J.Org。化学。,2007, 72,5867-5869。

N-卤代琥珀酰亚胺在三氟甲磺酸和BF 3 -H 2 O中被有效活化,使得失活的芳族化合物发生卤化。BF 3 -H 2 O更经济,易于制备,不氧化,并提供足够高的酸度。
GKS Prakash,T。Mathew,D。Hoole,PM Esteves,Q。Wang,G。Rasul,GA Olah,J。Am。化学。SOC。, 2004年, 126,15770-15776。

芳基和杂芳基硼酸与N-碘代琥珀酰亚胺和 N-溴代琥珀酰亚胺反应,得到相应的碘 - 和溴 - 芳烃,产率良好。该反应通常是高度区域选择性的并且仅产生ipso-取代的产物。
C. Thiebes,GK苏里亚普拉卡什,NA Petasis,GA奥拉,SYNLETT, 1998年,141-142。

通过Rh(III)催化的CH键活化方法,发生不同类型芳族化合物 的高产,一般和实用的邻溴化和碘化反应。
N.Schröder,J。Wencel-Delord,F。Glorius,J。Am 。化学。SOC。,2012, 134,8298-8301。

使用氰基作为引导基团,钯催化的邻卤化(I,Br,Cl)反应产生良好至极好的产率。该方法与具有吸电子或给电子基团的芳基腈相容。本方法已成功应用于paucifloral F和isopaucifloral F.
B. Du,X。Jiang,P。Sun ,J.Org。的前体的合成。化学。,2013, 78,2786年至2791年。

从苯乙烯中 高度立体选择性一锅法合成(E)-β-芳基乙烯基碘化物和(E)-β-芳基乙烯基溴化物的有效方案是基于钌催化的甲硅烷基化偶联,然后是N-卤代琥珀酰亚胺介导的卤代硅烷化反应。
P.Pawluć,G。Hreczycho,J。Szudkowska,M。Kubicki,B。Marciniec,Org。快报。,2009年, 11,3390-3393。

使用三乙胺作为催化剂在Hunsdiecker反应中与N-卤代琥珀酰亚胺作为Br +或I +源,肉桂酸和丙炔酸在1-5分钟内以良好的分离产率转化为相应的α-卤代苯乙烯和1-卤代-1-炔烃。
J. Prakash,S。Roy,J。Org。化学。, 2002,67,7861-7864。

J. Prakash,S。Roy,J。Org。化学。, 2002,67,7861-7864。

在N-溴代琥珀酰亚胺和催化量的乙酸锂存在下,通过微波辐射相应的3-芳基丙烯酸,在短的反应时间(1-2分钟)内容易地制备 (E)-β-芳基乙烯基溴化物。 C.旷,问:杨H.仙北,德田M.,合成,2005年,1319-1325。

直接从炔丙醇中有效合成α-碘/溴-α,β-不饱和醛/酮是由Ph 3 PAuNTf 2 和MoO 2(acac)2协同催化的,Ph 3 PO作为添加剂有助于抑制不需要的烯酮/ enal形成。该方法的显着特征包括低催化剂负载,温和的反应条件,以及大多数良好的非对映选择性。
L. Ye,L。Zhang,Org。快报。,2009年, 11,3646-3649。

通过Rh(III)催化的CH-活化/卤化机理,在温和条件下进行区域选择性和立体选择性碘化以及溴化的一些实例。该反应代表了贫电子丙烯酸衍生物直接卤化以获得各种不同取代的Z-卤代丙烯酸衍生物的罕见实例。
N. Kuhl,N.Schröder,F。Glorius,Org。快报。,2013, 15,3860-3863。

在一个NBS-促进allyloxyl加成Claisen重排-脱溴化氢级联反应,超过20个取代alkynylsulfonamides用烯丙醇反应,生成(2 Ž以良好的收率)-2,4- dienamides。理论计算表明[3,3] sigmatropic重排是限速步骤。
R. Ding,Y。Li,C。Tao,B。Cheng,H。Zhai,Org。快报。, 2015年, 17,3994-3997。

快速方便的一步法可在室温下在非常温和的条件下以高产率使用NBS-Et 3 N•3 HBr在碳酸钾存在下将α,β-不饱和羰基化合物转化为相应的溴代烯酮在二氯甲烷中
D.此Jyothi,S. HariPrasad,SYNLETT,2009年,2309-2311。

使用氨腈作为氮源和NBS作为氧化剂的醛的温和的一锅氰基亚胺化以高产率实现,而无需添加催化剂。随后,取代的N-氰基苯亚氨酸酯产物也可以进行环化反应,以高产率得到1,2,4-三唑衍生物。
P. Yin,W.-B。Ma,Y。Chen,W.-C。Huang,Y。Deng,L。He,Org。快报。,2009年, 11,5482-5485。

Sm(OTf)3是一种有效的催化剂,用于多种有效的卤素促进的高区域和立体选择性Friedel-Crafts(FC)烷基化富电子芳烃与烯烃和α,β-不饱和羰基化合物在NBS存在下或我2作为卤素源。
S. Haira,B。Maji,S。Bar,Org。快报。,2007, 9,2783年至2786年。

简单的末端炔烃的新的银催化的高区域和立体选择性双官能化反应以良好的收率得到(Z)-β-卤代乙酸酯衍生物。所得产物是有机合成中的通用中间体。
Z. Chen,J。Li,H。Jiang,S。Zhu,Y。Li,C。Qi,Org。快报。,2010, 12,3262-3265。

氨基溴化烯烃的新方法使用Cu,Mn或V催化剂以对甲苯磺酰胺作为氮源和N-溴代琥珀酰亚胺(NBS)作为溴源,以高产率得到邻位的溴胺衍生物 。对于不同的烯烃底物以及过渡金属催化剂,显示出优异的区域和立体选择性。
VV Thakur,SK Talluri,A。Sudalai,Org。快报。,2003, 5,861-864。

在温和的条件下, 使用廉价的FeCl 2作为催化剂,酰胺/磺酰胺和NBS作为氮和溴源,已经开发了方便和有效的铁催化的烯烃氨基溴化反应。
Z.王,张Y.,H.富,Y.江,Y.赵,SYNLETT,2008,2667年至2668年。

在未活化的烯烃的有效,无催化剂和无金属的溴代酰胺化中,分别使用4-(三氟甲基)苯磺酰胺和N-溴代琥珀酰亚胺作为氮和卤素源。该方法适用于环状和脂肪族烯烃。
WZ Yu,F。Chen,YA Cheng,Y.-Y。Yeung,J。Org。化学。, 2015年, 80,2815年至2821年。

烯烃,氰化物,胺和N-溴代琥珀酰亚胺的新型亲电子一锅反应能够以非常好的产率合成许多胍衍生物 - 包括rTRTVI前体。
L. Zhou,J。Chen,J。Zhou,Y.-Y。Yeung,Org。快报。,2011, 13,5804-5807。

没有过渡金属催化剂的烯烃的立体选择性芳基化和乙烯基化通过在温和条件下有趣的NBS促进的半精氨酸重排和随后不寻常的NaOH介导的Grob片段化而发生。
D.-Y. 袁,Y.-Q。Tu,C.-A。范,J.Org。化学。,2008, 73,7797-7799。

使用烯烃,腈,胺和N-溴代琥珀酰亚胺的新型阳离子Br引发的一锅法合成得到咪唑啉,收率良好。可以灵活地改变烯属底物和腈配偶体以获得一系列咪唑啉衍生物。
L. Zhou,J。Zhou,CK Tan,J。Chen,Y.-Y。Yeung,Org。快报。,2011, 13,2448-2451。

甲Ñ的从开始2,5- diaryloxazoles溴代琥珀酰亚胺介导的直接合成Ñ -H通过在原位形成ketoaziridines前进Ñ -bromoketoaziridines随后代甲亚胺叶立德的。
HS Samimi,F. Dadvar, 合成,2015年,47,1899-1904。

作为易得的合成中间体的3-恶唑啉-4-羧酸酯可被氧化以产生恶唑-4-羧酸酯。此外,用格氏试剂衍生化3-恶唑啉-4-羧酸酯能够容易地制备4-酮 - 恶唑衍生物。
K. Murai,Y。Takahara,T。Matsushita,H。Komatsu,H。Fujioka,Org。快报。,2010, 12,3456-3459。

2-氨基-4-烷基 - 和2-氨基-4-芳基噻唑-5-羧酸酯及其辛烯唑类似物通过β-酮酯与N-溴代琥珀酰亚胺的α-卤化合成,然后分别用硫脲或硒脲环化,在β-环糊精存在下,在50℃的水中。
M. Narender,MS雷迪,VP库马尔,B. SRINIVAS,R.斯里达尔,YVD Nageswar,KR饶,合成,2007,3469-3472。
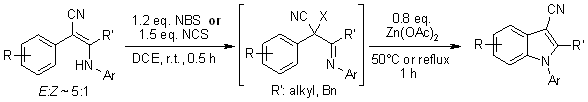
各种2-芳基-3-芳基氨基-2-烯腈通过NBS-或NCS-介导的卤化随后通过Zn(OAc)2催化的分子内环化以一锅方式得到N-芳基吲哚-3-碳腈。该方法包括形成芳基亚硝基离子中间体,其经历亲电芳族取代以得到环化的N-芳基吲哚。 Q. Yan,J。Luo,D。Zhang-Negrerie,H。Li,X。Qi,K。Zhao,J。Org。化学。,2011, 76,8690-8697。

叔丁基亚砜可以在磺酰胺的分子内亚磺酰化中用作亚磺酰基源,然后是全杂原子Wittig等价方法,以高产率得到芳基[4,5]异噻唑。
F. Xu,Y。Chen,E。Fan,Z。Sun,Org。快报。, 2016,18,2777年至2779年。

N-苯基重氮酰胺与N-卤代琥珀酰亚胺(NXS)的无催化剂的卤化环化反应在温和无催化剂条件下通过无卡宾机理以良好的收率提供3-卤代吲哚。提出该转化通过重氮离子形成,然后进行分子内Friedel-Crafts烷基化。
C. Ma,D。Xing,W。Hu,Org。快报。, 2016,18,3134-3137。

描述了使用醛,氨基醇和N-溴代琥珀酰亚胺作为氧化剂合成各种取代的2-恶唑啉和一种二氢恶嗪的新方法。该一锅法合成的特征在于反应条件温和,范围广,产率高,制备简单。
K. Schwekendiek,F Glorius, 合成,2006年,2996-3002。

β-氨基 - 炔酮中间体的金催化环化和卤化反应过程能够快速有效地一步合成卤代吡啶酮。
KH Nguyen,S。Tomasi,M。Le Roch,L。Toupet,J。Renault,P。Uriac,N。Gouault,J。Org。化学。,2013, 78,7809-7815。

多官能且高效的Zn(OTf)2催化的烯烃,NBS,腈和TMSN 3的一锅反应得到各种1,5-二取代的四唑,其含有另外的N-烷基取代基的α-溴官能团。
S. Hajra,D。Sinha,M。Bhowmick,J。Org。化学。,2007, 72,1852年至1855年。

描述了从伯醇中一锅法合成芳基砜。用N-溴代琥珀酰亚胺和三苯基膦处理醇,然后加入亚砜酸钠和催化量的四丁基碘化铵,得到芳基砜,产率高至高。
T.村上,K.古泽,合成, 2002年,479-482。

带有叔丁基的亚砜可以在酸性条件下使用N-溴代琥珀酰亚胺(NBS)活化。随后用各种氮,碳或氧亲核试剂处理,得到各种亚磺酸酰胺,新亚砜和亚磺酸酯。
J. Wei,Z。Sun,Org。快报。, 2015年, 17,5396-5399。

通过铜催化的有氧二聚化合成的硫代磺酸盐用作生产各种砜和磺酰胺的简单和高产率策略的底物。硫代亚磺酸盐是源自有毒SO 2的金属亚磺酸盐的稳定,无毒的替代品。
PK Shyam,H.-Y。Jang,J。Org。化学。, 2017,82,1761年至1767年。

N-氰基硫亚胺 的合成可以通过在碱和NBS或I 2作为卤化剂存在下使相应的硫化物与氰胺反应而容易地实现。氧化然后脱氰,得到合成有用的亚砜亚胺。
O.GarcíaMancheño,O。Bistri,C。Bolm,Org。快报。,2007, 9,3809-3811。

在一锅法级联酮转化为α-咪啶酮中,N-溴代琥珀酰亚胺(NBS)提供亲电子溴和亲核氮源,二氮杂双环[5.4.1]十一碳-7-烯(DBU)作为碱和亲核启动子用于激活NBS。α-溴化被认为是该过程中的关键步骤。
Y. Wei,S。Lin,F。Liang,Org。快报。,2012, 14,4202-4205。


目前评论:0